Artistieke weergawe van sterwende selle wat hul bure beskerm om weefselintegriteit te handhaaf. Gate in epiteel wat deur ongekoördineerde seldood geskep word, word in pers getoon. Krediet: © Institut Pasteur / Léo Valon et Romain Levayer
Selle wat seldood ondergaan, beskerm hul bure om weefselintegriteit te handhaaf.
Om weefselvernuwing moontlik te maak, skakel menslike weefsels voortdurend miljoene selle uit, sonder om weefselintegriteit, vorm en konnektiwiteit in gevaar te stel. Die meganismes betrokke by die handhawing van hierdie integriteit bly onbekend. Wetenskaplikes van die Institut Pasteur en die CNRS het onlangs 'n nuwe proses onthul wat uitgeskakelde selle toelaat om hul bure tydelik teen seldood te beskerm en sodoende weefselintegriteit te behou. Hierdie beskermende meganisme is noodsaaklik, en as dit ontwrig word, kan dit lei tot 'n tydelike verlies van konnektiwiteit. Die wetenskaplikes het opgemerk dat wanneer die meganisme gedeaktiveer word, die gelyktydige uitskakeling van verskeie naburige selle weefselintegriteit benadeel. Hierdie gebrek aan integriteit kan verantwoordelik wees vir chroniese inflammasie. Die resultate van die navorsing is in die joernaal gepubliseer Ontwikkelingsel on June 2, 2021,.
Menslike epitelia is weefsels wat in verskeie dele van die liggaam voorkom (soos die epidermis en interne mukosa). Hulle is saamgestel uit lae aangrensende selle wat dien as 'n fisiese en chemiese versperring. Hierdie rol word voortdurend deur beide die buite-omgewing en hul eie vernuwing op die proef gestel. Weefselvernuwing behels die vorming van nuwe selle deur seldeling en die uitskakeling van dooie selle. Die meganismes wat die vermoë van epitelia reguleer om hul integriteit te handhaaf in kontekste wat groot getalle geëlimineerde selle behels, bly swak verstaan, ten spyte van die feit dat hierdie situasie gereeld voorkom tydens embriogenese of die instandhouding van volwasse weefsels. Byvoorbeeld, meer as tien biljoen selle kan elke dag in 'n volwasse ingewande uitgeskakel word. Hoe word hierdie eliminasies georkestreer om weefselintegriteit en konnektiwiteit te handhaaf?
Wetenskaplikes van die Institut Pasteur en die CNRS het daarop gemik om die meganismes betrokke by epiteelintegriteit en die toestande wat epiteelverbindings kan beïnvloed te identifiseer deur Drosophila (of asynvlieë) te gebruik, 'n organisme wat in die laboratorium bestudeer is met 'n soortgelyke epiteel-argitektuur as mense.
Deur proteïensensitiewe fluoresserende merkers te gebruik, het die navorsingspan aan die lig gebring dat wanneer 'n sel sterf, die EGFR-ERK-weg – 'n selaktiveringsseinweg wat bekend is vir sy betrokkenheid by die regulering van seloorlewing – tydelik in die naburige selle geaktiveer word. Die wetenskaplikes het opgemerk dat die aktivering van die EGFR-ERK-weg naburige selle vir ongeveer een uur teen seldood beskerm het, en sodoende die gelyktydige eliminasie van 'n groep selle voorkom. "Ons het reeds geweet dat hierdie pad 'n sleutelrol speel in die regulering van seloorlewing in epiteelweefsel, maar ons was verbaas om sulke beskermende dinamika tussen selle waar te neem," sê Romain Levayer, Hoof van die Sel Dood en Epiteel Homeostase Eenheid by die Institut Pasteur en laaste skrywer van die studie.
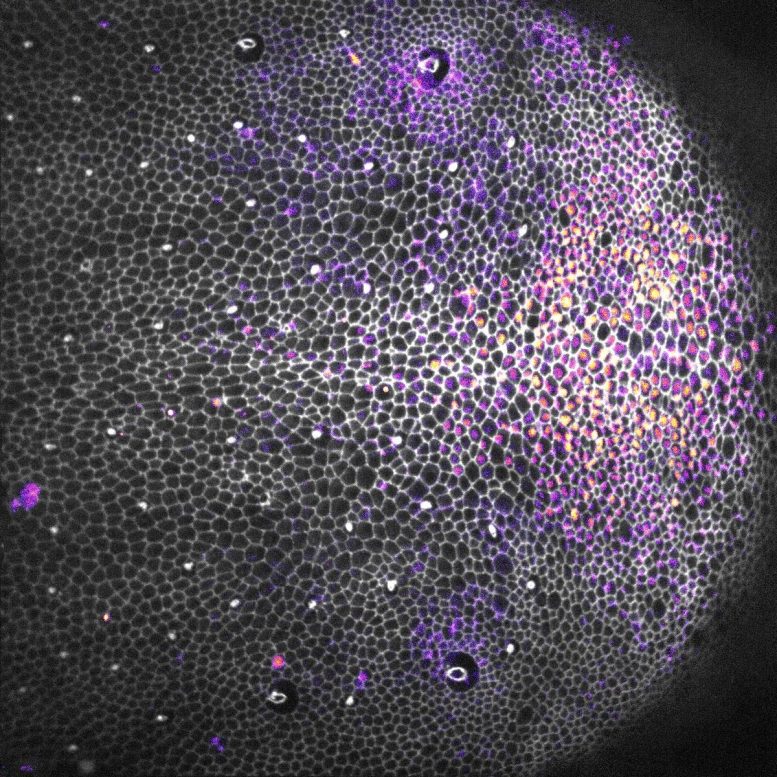
'n Drosophila papie-epiteel wat selkontoere (grys) toon en die verslaggewer van die EGFR-ERK-baan (geel/pers gradiënt). Krediet: © Institut Pasteur / Romain Levayer et Léo Valon
Die wetenskaplikes se navorsing toon ook dat die inhibering van hierdie beskermende meganisme 'n drastiese uitwerking op epiteelweefsel het: seluitskakeling word lukraak en naburige selle kan gelyktydig uitgeskakel word, wat lei tot herhaalde verliese aan konnektiwiteit. Die eliminasie van groepe naburige selle word nooit in epiteelweefsel waargeneem in normale toestande, wanneer die EGFR-ERK pad nie doelbewus geïnhibeer word nie, selfs al word 'n groot aantal selle uitgeskakel.
Deur 'n nuwe optogenetiese instrument te gebruik wat seldood in tyd en ruimte kan beheer en die beskermende meganisme kan omseil, het die wetenskaplikes bevestig dat epiteelintegriteit gekompromitteer is wanneer naburige selle gelyktydig uitgeskakel is. “Verbasend genoeg is epiteelweefsel hoogs sensitief vir die ruimtelike verspreiding van geëlimineerde selle. Alhoewel dit die uitskakeling van 'n groot aantal selle kan weerstaan, word epiteelintegriteit aangetas as net drie naburige selle gelyktydig uitgeskakel word,” verduidelik Léo Valon, 'n wetenskaplike in die Sel Dood en Epiteel Homeostase Eenheid by die Institut Pasteur en eerste skrywer van die studeer.
Die wetenskaplikes se waarnemings bevestig dat weefsels meganismes moet ontwikkel wat die uitskakeling van naburige groepe selle voorkom. “Hierdie waarnemings is belangrik aangesien dit die ongelooflike selforganiserende vermoë van biologiese weefsels illustreer, 'n eienskap wat hulle in staat stel om stresvolle toestande te weerstaan. Dit is dus nie nodig vir 'n dirigent om te orkestreer waar en wanneer die selle moet sterf nie; alles is gebaseer op hoogs plaaslike kommunikasie tussen naburige selle,” voeg Romain Levayer by.
Dit lyk asof hierdie proses tydens evolusie bewaar gebly het. Dieselfde beskermende meganisme gebaseer op plaaslike EGFR-ERK aktivering is onafhanklik in menslike sellyne ontdek deur die navorsingsgroep gelei deur Olivier Pertz aan die Universiteit van Bern in Switserland (die resultate word in dieselfde tydskrif gepubliseer2). Die resultate van die ander studie dui daarop dat die beskermingsmeganisme bewaar word tussen spesies wat deur honderde miljoene jare geskei word, wat aandui dat dit 'n relatief universele meganisme is.
Toekomstige navorsing sal aan die lig bring of ontwrigting van hierdie seldood-koördinasiemeganisme en herhaalde verlies aan konnektiwiteit in epiteelweefsel een van die wortels van chroniese inflammasie kan wees, 'n verskynsel wat verantwoordelik is vir verskeie siektes wat tans onder die hoofoorsake van dood wêreldwyd is.
Verspreiding van selderftes in 'n Drosophila-epiteel:
Ontwikkeling van die Drosophila papie-epiteel wat die ligging van alle selderftes (gekleurde kolletjies) toon. Die selkontoere word in grys getoon. Krediet: © Institut Pasteur / Léo Valon et Romain Levayer
Aktivering van die EGFR-ERK pad in naburige selle:
Aktivering van die EGFR-ERK-baan in die bure van 'n sel wat uit die weefsel geëkstrueer is. Die verslaggewer aan die linkerkant word uit die kern uitgesluit wanneer die pad geaktiveer word (die uitgeskakelde sel is in groen omsirkel). Aktivering kan ook deur ander padsensors bekyk word (die FRET-sensor – rooi vir sterk aktivering. Krediet: © Institut Pasteur / Romain Levayer et Léo Valon
Verwysings:
- "Robuustheid van epiteelafdichting is 'n opkomende eienskap van plaaslike ERK-terugvoer wat deur seluitskakeling gedryf word" deur Léo Valon, Anđela Davidović, Florence Levillayer, Alexis Villars, Mathilde Chouly, Fabiana Cerqueira-Campos en Romain Levayer, 2 Junie 2021, Ontwikkelingsel.
DOI: 10.1016/j.devcel.2021.05.006 - “Kollektiewe ERK/Akt-aktiwiteitsgolwe orkestreer epiteel-homeostase deur apoptose-geïnduseerde oorlewing aan te dryf” deur Paolo Armando Gagliardi, Maciej Dobrzyński, Marc-Antoine Jacques, Coralie Dessauges, Pascal Ender, Yannick Blum, Robert M. Hughes en Olivier Cohen. Pertz, 2 Junie 2021, Ontwikkelingsel.
DOI: 10.1016/j.devcel.2021.05.007
Hierdie navorsingsprojek is ondersteun deur die Europese Navorsingsraad (ERC), 'n Marie Skłodowska-Curie postdoktorale genootskap, die Fondation pour la Recherche Médicale (FRM) en die Cercle Fondation Schlumberger pour l'Education et la Recherche (FSER), R.Levayer 2019-pryswenner.






